Biliarna ciroza: klasifikacija, uzroci, simptomi. Primarna bilijarna ciroza.
Biliarna ciroza je poseban oblik ciroze (zamjena normalnog jetrenog vlaknastog tkiva i vezivnog tkiva). Vodeći uzrok njegovog nastanka je dugotrajno oštećenje bilijarnog trakta i prisutnost sindroma kolestaze - povreda ili prekid protoka žuči.
Postoje dva oblika bolesti:
Koje su terapijske indikacije?
U nekim slučajevima plazmafereza ima hitnu indikaciju koja pomaže u prevladavanju kritičnog stanja pacijenta. To je najsigurnija metoda bez detoksikacije tijela nuspojave kemijska obrada. Terapija plazmaferezom koristi se ovisno o kontekstu bolesti, i samostalno i povezano s klasičnom terapijom, s hitnom ili potpornom indikacijom koja omogućuje pacijentu ili ozlijeđenom organu da prevlada kritičnu situaciju.
Ovisno o etiopatogenim znakovima koristi se plazmafereza. Sindrom preosjetljivosti. Uklanjanje toksičnih tvari. Neonatalna hiperbilirubinemija. Eklampsija. Kao hitna terapija, ponekad plazmafereza postaje vitalna terapijska potreba.
- osnovni bilijalna ciroza jetre.
- Sekundarna bilijarna ciroza.
Ovi oblici bilijarne ciroze razlikuju se u svojim uzrocima i kliničkim manifestacijama, a također imaju različite strategije liječenja.
PBCP je polagano progresivna bolest jetre, čiji su pokretači za razvoj autoimunih poremećaja.
Autoimune bolesti s visokim titrom cirkulirajućih antitijela. S plazmaferezom brzo ispravlja hipervozorni sindrom, uklanja kolesterol, krioglobuline i djeluje protiv starenja. Profil seruma štetnih faktora i normalnih komponenata plazme značajno varira ne samo od jednog pacijenta do drugog, nego i od istog pacijenta do istog pacijenta, od jedne do druge sesije. Dakle, količina izmjene plazme određena je njihovim "kritičnim pragovima", koji žele smanjiti vrijednosti štetnog faktora ispod kritičnog praga i što manje utjecati na normalne komponente plazme.
Najviše žena u dobi od 40 godina.
Prevalencija bolesti je mala i prema mišljenju različitih istraživača od 25 do 150 slučajeva na milijun ljudi. Učestalost PBTsP u strukturi ciroze je oko 7-11%.
Bolest je prvi put opisana sredinom XI. Stoljeća, kada su znanstvenici uočili povezanost između pojave nodularnih formacija (xantham) i.
Individualni tretman Liječenje skleroze s plazmaferezom će biti individualizirano, kao i svaka druga terapija lijekovima. Sjednice se ponavljaju svaki drugi dan ili 2 dana, ovisno o kemijskoj i fiziološkoj strukturi ciljanog toksičnog faktora. Trajanje sesije je 1 sat i 30 minuta. Sjednica se provodi kroz venski pristup nekih vena na ruci s iglom potrebnom za pacijenta. Setovi su zapečaćeni, sterilni, jednokratni.
Vrlo je važno da se ti podaci izračunaju što točnije za svakog pacijenta. Napominjemo da je gubitak krvnih stanica neznatan, jer je separator opremljen fotonaponskom ćelijom, koja redefinira kritični trenutak odvajanja plazme.
Također treba napomenuti da u ranoj fazi bolesti nema znakova kroničnog kolangitisa (upale žučnih putova) bez. Stoga, neki znanstvenici dovode u pitanje ispravnost formulacije dijagnoze primarne bilijarne ciroze.
Razlozi za formiranje PTSP-a
Danas ove vrste separatora koriste sve banke krvi u zemlji za odvajanje plazme za proizvodnju lijekova za transfuziju. Periferna ciroza je rezultat netretiranog virusnog hepatitisa ili koji nije reagirao na liječenje, uporabu alkohola ili autoimune bolesti; Bolest obično ne uzrokuje bol, najbolje je liječiti hepatolog ili gastroenterolog, a uz pravilnu prehranu i liječenje opstanak može trajati desetljećima.
Životni vijek ciroze jetre. Dekompenzirana ciroza jetre znači ciroza s ascitesom? Ciroza je završni stadij kronične bolesti jetre s nepovoljnim ishodom. Ovo kronično, nepovratno emitiranje, karakterizira zamjena normalne arhitekture jetre hepatocitima regenerativnih čvorića okruženih vlaknastim septama. Arhitektonska dezorganizacija dovodi do jetrenog parenhimnog i vaskularnog.
Etiologija bolesti još nije poznata.
Vrlo često se kod provođenja ankete u bolesnika s PBCP otkrivaju različite autoimune bolesti. To nam omogućuje da izrazimo teoriju oslabljene imunološke regulacije u tijelu. U prilog ovoj teoriji su i duboki autoimuni poremećaji identificirani u laboratorijskim istraživanjima takvih pacijenata.
Etiologija ciroze jetre: kronični virusni hepatitis, kronični alkoholizam, autoimuni hepatitis, autoimuna destrukcija bilijarnih kanalića, stadij bilijara, cistična fibroza, hemokromatoza, Wilsonova bolest, alfa-1 antitripsin. Sekularna bilijarna ciroza javlja se zbog stagnacije žučnih proizvoda ekstrahepatične bilijarne opstrukcije. Značajke nodula regenerirajućih hepatocita, okruženih fibroznim septama. U regenerativnim čvorištima hepatociti su anarhični. To je bio: port-bilijarni prostor, žarišna vena centroafina i radijalni raspored hepatocita.
Kao rezultat autoimune reakcije dolazi do progresivnog razaranja (uništenja) žučnih puteva jetre. Nakon toga dolazi do njihove zamjene i okolnog jetrenog parenhima vlaknastim i vezivnim tkivom.
Pretpostavlja se da su pokretački mehanizmi autoimune reakcije bakterijski ili virusni agensi.
Uloga hormonskih čimbenika nije isključena, uzimajući u obzir prevladavajuću učestalost bolesti u žena.
U septama se nalaze kolagenska fibroza, smanjeni upalni infiltrat i brojni su žučni kanalići: neki su povrijeđeni, drugi hiperplastični ili neoplazmi, drugi oslabljeni, koji sadrže žučne ugruške. Sekundarna bilijarna ciroza.
Hepatocitni regenerativni čvorići okruženi fibroznim septama. Fibrosis septa sadrži kolagena vlakna, smanjenje mononuklearnog upalnog infiltrata i brojnih žučnih kanala žuči s novim ugruškom krvi unutar. Prikazujemo slučaj žene s novom dijagnozom adenokarcinoma želuca, za koju je utvrđeno da ima multifokalnu metastazu u jetri tijekom rutinske dijagnostičke transjugularne biopsije jetre. Detekcija metastatske bolesti u prisustvu ciroze je neočekivani nalaz koji negativno utječe na upotrebu citotoksičnih kemoterapeutskih sredstava.
Neki znanstvenici ne isključuju utjecaj genetskih i nasljednih čimbenika.
Autoimuna reakcija s PBCP
Uz ovo stanje, ljudsko tijelo počinje proizvoditi zaštitna antitijela protiv stanica vlastitog organa (autoantitijela). U ovom slučaju, protiv stanica žučnih kanala.
Normalno, antitijela se vežu na strani antigen da bi se stvorio imunološki kompleks, koji zatim tijelo uništava. U slučaju autoimune reakcije, stanice vlastitog tijela uzimaju se za strani antigen.
Ciroza korelira s ekstrahepatičnim malignim neoplazmama, uključujući rak želuca, koji mijenja terapijske mogućnosti. Međutim, dokaz metastatske bolesti u cirotičnoj jetri je rijedak nalaz zbog činjenice da je to nepovoljno mjesto za malignu invaziju. Izvanhepatični maligni tumori metastatski u cirotičnu jetru su manje uobičajeni zbog promjena u gradijentu toka portala i mogućih promjena u staničnom mikrookruženju.
Autoantitijela nastala kao odgovor na to vezuju se za proteinske molekule organskih stanica. Kao rezultat formiranja autoimunih kompleksa, stanice ciljnog organa su uništene. U našem slučaju, ovaj ciljni organ je žučni kanal. Nastaje destruktivni kolangitis, kao rana manifestacija ove bolesti. Nakon toga dolazi do razaranja stanica žučnog kanala i uključivanje parenhima u jetru. Na kraju, rezultat takvih patoloških promjena bit će ciroza jetre.
Znala je da boluje od jetre, ali nakon dijagnoze nije je slijedila. Nije imala povijest upotrebe alkohola, transfuziju krvi ili povijest intravenske uporabe droga. Pacijentica je hospitalizirana 1 mjesec prije prezentacije s boli u trbuhu, anemijom i povećanjem edema donjeg ekstremiteta. U prethodnoj studiji provedena je ezofagogastroduodenoskopija koja je pokazala ulceraciju želuca s biopsijama u skladu s slabo diferenciranim adenokarcinomom i magnetskom rezonancijom bez kontrasta, što upućuje na popratnu cirotičnu jetru s višestrukim mutnim heterogenim lezijama.
Morfološki se razlikuju četiri faze ove bolesti:
- Kronični ne-gnojni destruktivni kolangitis - zahvaćeni su samo žučni kanali jetre.
- Progresija destruktivnih procesa u žučnim kanalima, formiranje žarišta fibrozne transformacije oko njih. Razvijaju se znakovi kolestaze.
- Oštećeno je tkivo jetre, razvija se masivna fibroza, približava se žučnih putova, deformira. Izraženi znakovi kolestaze.
- Ciroza jetre.
Rani simptomi

Fizikalni pregled pacijenta zabilježen je istezanjem trbušne šupljine s promjenjivom tuposti. Uzimajući u obzir karakteristike slike koje ukazuju na cirozu, izvršena je transjugularna biopsija jetre. U uzorku biopsije jetre bilo je malih žarišta metastatskog adenokarcinoma s područjima limfovaskularne invazije na pozadini mikronodularne ciroze i fokalne sinusoidne fibroze. Pregled izvornih uzoraka želučane biopsije pokazao je slabo diferencirani adenokarcinom, koji se pojavio na pozadini atrofičnog gastritisa s intestinalnom metaplazijom.
Primarna bilijarna ciroza u početna faza oko 20% slučajeva su asimptomatski. Bolest se može posumnjati samo na temelju laboratorijskih rezultata.
Najraniji klinički simptom je pruritus, koji se javlja kod gotovo svih bolesnika.
Prvo, to se događa periodično, onda je stalno prisutno. Povećava se nakon toplinskih učinaka, kao što su tuš ili kada, te noću.
S obzirom na neočekivano otkrivanje metastatskog multifokalnog adenokarcinoma želuca u formulaciji ciroze, daljnja dijagnoza nije provedena, budući da su terapijske mogućnosti bile ograničene. Pacijentica je upućena na onkologiju, koja preporučuje palijativnu terapiju, uključujući fluorouracil i trastuzumab.
Najčešći simptomi uključuju gubitak težine, bol u trbuhu i mučninu, a najčešći klinički znak je anemija. Početno širenje bolesti može se dogoditi putem limfnog i hematogenog širenja, a jetra je najčešće zahvaćeni organ duž hematogene rute.
Pruritusu obično prethodi žutica. Međutim, to može biti jedini simptom za mnoge mjesece, pa čak i godine. U tom slučaju postoje pogrešne dijagnoze, a osoba može biti dugotrajna i neuspješno liječena od strane specijaliste bolesti kože (Dermatologa).
Mehanička ili kolestatska žutica se obično razvija polako. Intenzitet ikteričnog bojenja kože obično mali. Ponekad se čak i sclera može naslikati. Pojavljuje se u oko polovice bolesnika na početku bolesti.
Različite su studije potvrdile povećani rizik od raka jetre u bolesnika s cirozom. Nacionalna kohortna studija iz Danske pokazala je standardiziranu stopu incidencije od 9 za dijagnozu raka želuca u bolesnika s cirozom. Talijanska retrospektivna skupina bolesnika s probirom ciroze za portalnu hipertenziju pokazala je 6 puta veći rizik od razvoja raka želuca u usporedbi s procijenjenim rizikom za cijelu populaciju.
Iako je ciroza u korelaciji s povećanim rizikom od ekstrahepatičnih malignih tumora, pokazivanje metastatske bolesti u cirotičnoj jetri ostaje rijedak nalaz. Sustavni pregled 11 postmortemskih istraživanja pokazao je da je sirova stopa metastatskog širenja ekstrahepatičnog maligniteta za cirotičnu jetru smanjena u usporedbi s učestalošću metastatskog širenja u ne-cirotičnoj jetri. Hipoteze koje objašnjavaju ovo smanjenje uključuju prekid protoka portalne krvi, što dovodi do razvoja porto-sistemskog ranžiranja, gubitka endotelnih fenestacija s cirozom, stvarajući fizičku barijeru invaziji tumorskih stanica i promjene u ekspresiji adhezijskih molekula i mikrookruženja citokina.
Oko 60% bolesnika ima hiperpigmentaciju kože. Prvo, obično je lokaliziran između lopatica, a zatim se širi na druga područja kože.
Jedna trećina pacijenata ima kvrge - ksantome (na kapcima i oko očiju, nazivaju se ksantelazme), koje su nakupine masnoće u koži koje se događaju nakon poremećaja metabolizma lipida.
Naš slučaj pokazuje rijedak nalaz metastatskog adenokarcinoma želuca, koji je cirotična jetra. Nalazi ascitesa pripisani su ascitesu na portalnu hipertenziju. Promatranje metastatskog adenokarcinoma želuca u cirotičnoj jetri je rijedak nalaz iu tom slučaju ograničava terapeutske mogućnosti za palijativno liječenje.
Zhao je pripremio rukopis i pripremio brojke. Financijska objava: Nemojte nikome reći. Za ovo izvješće dobiven je informirani pristanak. Rizik od raka jetre i drugih raka u bolesnika s cirozom: nacionalna kohortna studija u Danskoj.
Takozvani jetreni znakovi - vaskularne "zvijezde", eritem (crvenilo) dlanova i drugi - iznimno su rijetki. Kod muškaraca se često otkriva ginekomastija - povećanje mliječnih žlijezda.
Povećana jetra opažena je u gotovo svih bolesnika. Obično je neozbiljan, au fazi remisije jetra se čak može smanjiti na gotovo normalnu veličinu.
Tromboza portalnih vena smatra se čestom komplikacijom ciroze jetre. Ključne riječi: tromboza portalnih vena, ciroza jetre, trombofilni čimbenici, antikoagulacija, splenektomija. Tromboza portalne vene, opstrukcija portalne vene ili njenih grana krvnim ugruškom javlja se u različitim kliničkim uvjetima, kao što su mijeloproliferativna bolest, ciroza, rak i infekcija.
Svaki od njih je uzastopna faza iste bolesti. Iako imaju slične razloge, razlikuju se u odnosu na upravljanje. Okluzija može biti potpuna ili djelomična, ostavljajući periferni cirkulirajući kanal. Broj, veličina i mjesto tih depozita uvelike variraju od pacijenta do pacijenta.
Slezena je uvećana u više od polovice slučajeva i, poput jetre, može se smanjiti u fazi remisije.
Često zabrinuti zbog bolova u kostima, zglobovima, donjem dijelu leđa, što ukazuje na proces demineralizacije koštanog tkiva.
Gotovo se uvijek primjećuju nespecifični simptomi kao što su bol u desnom hipohondriju, manifestacije dispeptičkog sindroma (mučnina, povraćanje, nadutost, poremećaji stolice itd.). Često se temperatura tijela povećava, sve do groznice.
Nedavno se ciroza smatrala hiperkoagulabilnim stanjem, a ne hipokogagulacijskim stanjem. U bolesnika s cirozom jetre smanjene su razine pro i antikoagulantnih proteina u uvjetima zatajenja jetre. Krajnji rezultat je hemostatska ravnoteža, koja se kompenzira u normalnim okolnostima, bez sklonosti krvarenju ili trombozi.
Međutim, u bolesnika s oštećenom funkcijom sinteze i niskim razinama inhibitora prirodne koagulacije plazme, trenutno ne postoji jednostavan način da se ta niska razina pripiše prethodno postojećem deficitu. Amitrano i sur. Pretpostavili su da je zastoj krvi kod bolesnika s cirozom velika promjena koja pogoduje trombozi, čak i kod drugih lokalnih, sistemskih, kongenitalnih i stečenih čimbenika.
Utvrđeni su simptomi asteno-vegetativnog sindroma: slabost, poremećaji apetita, umor itd.
Simptomi kasne faze

Stanje se pogoršava, povećava se žutica, povećavaju se manifestacije dispeptičnog i asteno-vegetativnog sindroma. Tjelesna temperatura može doseći visoke vrijednosti.
Intenzitet pruritusa napreduje. Međutim, u terminalnom stadiju slabi, a s razvojem zatajenja jetre može potpuno nestati. Prema tome, smanjenje manifestacije ovog simptoma, paradoksalno, je loš prognostički znak.
Stanje kože se mijenja. Na mjestima hiperpigmentacije ona se zgusne i zgusne do gustog edema, posebno izraženog na dlanovima i stopalima. tamo različitih vrsta osip. Mogu postojati žarišta depigmentacije - sijeva koža, slična vitiligu.
Zbog kršenja sekrecije žuči i funkcioniranja crijeva razvija se sindrom malabsorpcije. To ometa apsorpciju vitamina, osobito masno topljivih (A, D, E, K), minerala i hranjivih tvari. Pojavljuju se česti, tekući i masni izmet, žeđ, suha koža i sluznice. Zbog nedostatka apsorpcije kalcija i drugih minerala nastaje osteoporoza - krhkost kostiju, zubi su oštećeni i ispadaju. Iscrpljenost se razvija, ponekad vrlo izražena.
Razvija se portalna hipertenzija, čiji je jedan od znakova proširene vene jednjaka i želuca.
Zbog abnormalnih funkcija jetre stvara se hemoragijski sindrom koji se manifestira krvarenjem. Uključujući gastrointestinalne i proširene vene jednjaka.
Veličina jetre se povećava, au nekim slučajevima postaje ogromna. Postoji povećanje i slezena.
Jedna od strašnih kasnih komplikacija PBCP-a je razvoj karcinoma žučnih kanala - kolangiokarcinom, kao i zatajenje jetre.
Povezane manifestacije

Primarnu bilijarnu cirozu karakteriziraju i lezije organskih sustava.
Kod gotovo svih bolesnika, tijekom ciljanog pregleda otkriven je specifičan pregled kože, sluznica i salivarnih i suznih žlijezda - Sjogrenov sindrom. Ovaj se sindrom odlikuje suhom kožom, smanjenim suzenjem i, kao posljedicom, oštećenjem konjunktive i rožnice oka. Također je otkrivena kronična lezija žlijezda slinovnica - parotitis i druge manifestacije. Proces širenja uključuje sluznicu nosa, ždrijela, grkljana, dušnika, bronha, organa gastrointestinalnog trakta (GIT), itd.
Gastrointestinalne lezije se manifestiraju u disfunkciji duodenalnog i tankog crijeva zbog povrede žučnog toka. Također postoji nedostatak funkcije izlučivanja gušterače.
Neispravnosti endokrinog sustava kod žena otkrivene su kao povreda funkcije jajnika. Često se primarna bilijarna ciroza razvija u menopauzi ili nakon poroda ili pobačaja. Rijetko postoji hipotalamička insuficijencija, smanjena funkcija nadbubrežne kore.
Moguće su i patološke promjene u bubrezima i krvnim žilama (vaskulitis).
Često, različita autoimuna stanja kao što su sklerodermija, reumatoidni artritis, Hashimoto tireoiditis, mijastenija itd.
Najčešće, primarna bilijarna ciroza javlja se u kombinaciji s autoimunim bolestima štitnjače - u 23–31% slučajeva. Na drugom mjestu su skleroderma i reumatoidni artritis.
Treba primijetiti statistički čestu pojavu ekstrahepatičnih karcinoma u bolesnika s PBCP. Rak dojke se često dijagnosticira kod žena, a Hodgkinov sarkom (limfogranulomatoza) kod muškaraca. Najvjerojatnije je karcinogeneza povezana s oslabljenim imunološkim odgovorom i imunodeficijencijom, što je karakteristično za PBCP.
dijagnostika
osim toga kliničke manifestacije treba razmotriti laboratorijska i instrumentalna ispitivanja.
Kod dijagnosticiranja krvi u ranom stadiju PBCP otkriveno je povećanje ESR-a i povećanje aktivnosti markerskih enzima kolestaze: alkalne fosfataze (ALP), gama-glutamil transferaze (GGT), leucin aminopeptidaze i 5-nukleotidaze.
Otkrivaju se poremećaji metabolizma lipida: izražena hiperlipidemija s prevladavajućim porastom razine kolesterola i drugim promjenama.
Povećanje razine bilirubina u krvi je usporeno. Međutim, u kasnijoj fazi, povećanje njegove koncentracije može premašiti normu za faktor deset ili više. Razina žučnih kiselina raste.
Važna važnost u dijagnostici PBTsP daje se za identifikaciju anti-mitohondrijskih antitijela (AMA). Ta antitijela tijelo proizvodi na vlastite stanične komponente (mitohondrije). Postoji nekoliko vrsta antigena (M1-M9), koje proizvodi AMA, međutim, definicija anti-M2, a zatim anti-M4, M8, M9, klinički je važna u dijagnostici PBCP.
Antimitohondrijska protutijela često se određuju u predkliničkom stadiju i ne nestaju tijekom bolesti. Naslov dijagnoze smatra se 1:40 i višim.
Utvrđeno je izraženo povećanje razine gama globulina i koncentracije IgM. Razine IgG i IgA i imunih kompleksa koji cirkuliraju u krvi umjereno su povećani.
Instrumentalne metode ispitivanja, kao što su ultrazvuk, CT, MRI, omogućuju otkrivanje nepromijenjenih ekstrahepatičnih žučnih putova i osiguravaju da manifestacije bolesti nisu uzrokovane opstrukcijom (blokadom), na primjer, s kamenom.
Važna metoda za potvrdu dijagnoze je morfološka studija biopsije. Zbog toga je u kasnijoj fazi moguće dijagnosticirati ne-gnojni destruktivni holangitis u ranoj fazi bolesti i specifične manifestacije bilijarne ciroze.
liječenje

Liječenje PBCP-a je složeno i uključuje nekoliko principa: prehranu, simptomatsko liječenje i korekciju poremećaja u tijelu koji su uzrokovali razvoj bolesti.
U liječenju ove bolesti je vrlo važno pravilnu prehranu s unosom vitamina i minerala. Posebna pozornost treba unositi vitamine topljive u mastima - A, D, E, K.
Simptomatsko liječenje uključuje uporabu lijekova koji smanjuju intenzitet boli za kožu pacijenta. U tu svrhu koriste se kolestiramin, bilignin i drugi. Također se provodi korekcija insuficijencije enzima gušterače.
Kako bi utjecali na uzrok bolesti - oslabljen imunološki odgovor, upotrijebite lijekove koji imaju imunosupresivna, protuupalna, antifibrotička svojstva. Takvi lijekovi uključuju glukokortikoide, imunosupresive, citotoksične lijekove itd. Oni imaju mnogo nuspojava i kontraindikacija.
Preparati žučne kiseline - ursodeoksiholna kiselina (UDCA) i ademetionin su obećavajući agensi za liječenje PBCP zbog svoje učinkovitosti i minimalnih nuspojava.
Transplantacija jetre koristi se za progresiju bolesti s pojavom znakova dekompenzacije jetre. Ali u bolesnika s terminalnim zatajenjem jetre takva operacija nema smisla.
pogled
Prosječno očekivano trajanje života za asimptomatsku PBCP obično je 10-20 godina. Ako su kliničke manifestacije već prisutne, očekivano trajanje života gotovo je prepolovljeno na 7-10 godina.
Kada se izvrše transplantacije jetre, poboljšavaju se prognoza i kvaliteta života. Ako je uspješna, ovaj način liječenja može se povećati za deset godina ili više.
Sekundarna bilijarna ciroza
![]()
Ova bolest razvija zbog kršenja odljeva žuči kroz velike intrahepatic ili extrahepatic žučnih vodova za dugo vremena.
Muškarci se razbole gotovo dvostruko češće od žena. Starost oboljelih je obično 25-50 godina.
uzroci
Poremećaj normalnog kretanja žuči duž žučnih puteva može se pojaviti iz različitih razloga. Najčešća mehanička opstrukcija (blokada) lumena žučnih putova, koja nastaje kao rezultat:
- Nastajanje kamenja s žučnim kamencima.
- Maligni tumor gušterače i Vater papile.
- Ograničenja žučnih putova.
- Upalne bolesti žučnih putova (kolangitis).
- Benigni tumor, češće - ciste, zajednički žučni kanal.
- Suženja i opstrukcija žučnih putova nakon kirurških zahvata na njima, žučni mjehur ili jetre.
Promjene u protoku žuči mogu se također spriječiti promjenama u parenhimu jetre tijekom upalnih bolesti herpatitis. To uključuje:
- Toksični hepatitis, češće - lijek koji se pojavljuje kod uzimanja lijekova koji imaju hepatotoksični učinak.
- Virusni hepatitis, koji se razvija s oštećenjem jetre hepatotropnim virusima.
- Alkoholni hepatitis - zbog dugotrajne zlouporabe alkohola.
Rijetko, uzroci koji krše protok žuči mogu biti neke nasljedne bolesti i malformacije bilijarnog trakta, na primjer, atrezija - odsutnost ili prekomjerni rast žučnih putova.
Kod nekih extrahepatic bolesti, normalno kretanje žuči također može biti poremećeno: limfogranulomatoza, amiloidoza, cistična fibroza, itd.
Razvojni mehanizam
Uz dugoročno kršenje odljeva žuči duž žučnih puteva u jetri - kolestaza, pritisak u žučnim kanalima raste, dolazi do njihovog edema. Žuči se "istiskuju" u parenhim jetre oko kanala.
U tim područjima nastaje nekroza tkiva jetre, koja se zatim zamjenjuje fibroznim tkivom. Tijekom vremena razvija se cirotična degeneracija parenhima u jetri. Trajanje takve promjene može biti u rasponu od nekoliko mjeseci do pet godina.
Spajanje bakterijske infekcije, koja često komplicira proces stagnacije žuči, može ubrzati nastanak ciroze. Takva varijanta tijeka sekundarne bilijarne ciroze naziva se kolangiohepatitis (holangiogeni hepatitis, žučni hepatitis). Najčešće se holangiogeni hepatitis javlja kod komplicirane holelitijaze i strikture žučnih puteva.
Autoimuna reakcija ne igra ulogu u formiranju sekundarne bilijarne ciroze.
simptomi

Prije svega, kliničke manifestacije sekundarne bilijarne ciroze (VBCP) uzrokovane su bolešću koja je uzrokovala poremećaj u normalnom kretanju žuči duž žučnih puteva.
Međutim, mogu se razlikovati simptomi tipični za razvoj ciroze:
- Vodeće manifestacije UCPP-a su pruritus i žutica. Pruritus je već otkriven rane faze bolest. Isprva je to periodično, ali s progresijom razvoja ciroze ima stalan oblik.
- Ikretno bojenje kože i sluznice obično je intenzivno. Žutica ima mehanički (kolestatski) tip. Zajedno s žućkasto obojenje promjena boje kože na izmetu i zamračenje urina.
- Gotovo uvijek postoji dispeptički sindrom, koji se manifestira podrigivanjem, mučninom, povraćanjem i oslabljenom stolicom - često se javlja proljev.
- Postoje simptomi intoksikacije i asteno vegetativnog sindroma - povećanje tjelesne temperature, češće do subfebrilnog broja, slabosti, umora, smanjene učinkovitosti, itd. Smanjuje se tjelesna težina, sve do iscrpljenosti.
- Pristupanjem infekcije i formiranjem kolangiogenog hepatitisa, tjelesna temperatura može dosegnuti veliki broj, pojaviti se zimica i obilno znojenje. Takvi simptomi se u pravilu javljaju sporadično, u trajanju od nekoliko sati do nekoliko dana.
- Bolovi u desnoj hipohondriji su uvijek prisutni. Njegov intenzitet može biti različit: od osjećaja težine, nelagode u području jetre do pojave boli koja podsjeća na žučnu koliku.
- Kao posljedica kršenja hemostatske funkcije jetre, razvija se hemoragijski sindrom, karakteriziran krvarenjem.
- Utvrđeno je povećanje jetre - hepatomegalija. Jetra ima gustu teksturu i često je bolna na palpaciji. Povećana slezena je rjeđa, obično već u kasnoj fazi ciroze, kao jedan od znakova portalne hipertenzije.
Kasni znakovi uključuju znakove "jetre": telangiektazije (vaskularne "zvijezde"), crvenilo dlanova, rjeđe - tabane (palmarni eritem), dilataciju vena na prednjoj trbušnoj stijenci itd.
S progresijom ciroze javljaju se znakovi portalne hipertenzije. Najčešća manifestacija su proširene vene jednjaka, koje mogu biti komplicirane krvarenjem iz njih.
Terminalno stanje u tijeku sekundarne bilijarne ciroze je formiranje zatajenja jetre i njezina završna faza - jetrena koma.
Dijagnoza VBCP
Prilikom dijagnosticiranja na prvom mjestu treba uzeti u obzir prisutnost bolesti, koja ometa normalan protok žuči. U prošlosti mogu postojati indikacije prenesenih žučnih putova ili žučnog mjehura.
U laboratorijskim ispitivanjima, opći test krvi otkriva znakove upalne reakcije: povećanje leukocita, ubrzani ESR, itd. Takve promjene su najizraženije s razvojem kolangiogenog hepatitisa.
U općoj analizi bjelančevina mokraće može se otkriti, žučni pigmenti - bilirubin (koji boji urin u tamnoj boji).
U biokemijskoj analizi krvi, povećanje razine markera kolestaze: alkalne fosfataze, gama-glutamiltransferaze i drugih. Aktivnost alanin aminotransferaze (ALT) se povećava. Karakteristično je povećanje razine kolesterola, bilirubina zbog njegove konjugirane frakcije.
Promjene u proteinogramu (pokazatelji metabolizma proteina) uočene su: smanjenje razine albumina, povećanje alfa2 i gama globulina.
Instrumentalne metode ispitivanja su od neprocjenjive važnosti u otkrivanju uzroka kršenja odljeva žuči. Dakle, tijekom ultrazvučnog pregleda (ultrazvuk) hepatobilijarnog sustava može se otkriti kamenac, tumor, sužavanje žučnih putova. Kako bi se nadopunili podaci o opstrukciji žučnih kanala, provode se perkutana transhepatična holangiografija i retrogradna kolangiopankreatografija.
Za točnu dijagnozu koristi se punktirajuća biopsija jetre, nakon čega slijedi histološko ispitivanje biopsije.
Endoskopski pregled jednjaka i gornjeg dijela crijeva - (FEGDS), te rektum (rektomomanoskopija) koristi se za dijagnozu lezija ovih organa tijekom razvoja portalne hipertenzije u kasnim fazama sekundarne bilijarne ciroze.
Liječenje i prognoza života

Glavni cilj liječenja VBCP je uklanjanje prepreka normalnom kretanju žuči duž žučnih puteva. Za to se koristi kirurška intervencija. Glavne vrste operacija su:
- Holedochotomy - disekcija zida zajedničkog žučnog kanala (choledochus).
- Choledochostomy - nametanje umjetne fistule zajedničkog žučnog kanala s ciljem drenaže, obično u duodenumu.
- Uklanjanje kamenja iz bilijarnog trakta.
- Endoskopska bougienage - instrumentalna restauracija prohodnosti - suženja (strikture) žučnih kanala.
- Endoskopsko stentiranje (uspostavljanje posebnog okvira - stenta) zajedničkog žučnog kanala.
- Balonska dilatacija (ekspanzija) žučnih putova.
- Vanjska drenaža žučnih vodova.
Nakon uspješne kirurške korekcije uzroka koji je uzrokovao nastanak sekundarne bilijarne ciroze, stanje pacijenta značajno se poboljšava. Očekivano trajanje života za takve pacijente postaje povoljnije.
Ako je nemoguće ukloniti uzrok blokade žučnog sustava, pacijentima se propisuje simptomatska terapija. S obzirom na čest pristup infekcijama, razumno je koristiti antibakterijska sredstva.
Propisani lijekovi koji olakšavaju intenzitet pruritusa. U tijeku je terapija detoksikacije. Obavezno imenovanje multivitaminskih pripravaka s mikronutrijentima.
Indikacija za transplantaciju jetre je kasni stadij sekundarne bilijarne ciroze.
Primarna bilijarna ciroza (PBC) je polagano progresivna autoimuna bolest jetre koja se javlja uglavnom kod žena. Najčešće se bilijarna ciroza razvija u dobi od 40 do 50 godina i vrlo rijetko u osoba mlađih od 25 godina. Histološki pregled pokazuje upalne promjene u portalnim traktima i autoimuno razaranje intrahepatičkih žučnih putova. To dovodi do smanjenja protoka žuči i odgađanja otrovnih tvari u jetri, što je uzrok smanjene funkcije jetre, fibroze, ciroze i zatajenja jetre.
U primarnoj bilijarnoj cirozi pojavljuju se anti-mitohondrijska antitijela (u 90-95% bolesnika), često mnogo prije prvih kliničkih znakova bolesti. Neobjašnjiva značajka primarne bilijarne ciroze, kao i mnoge druge autoimune bolesti, jest da unatoč prisutnosti mitohondrija u svim stanicama tijela, patološki proces je ograničen na jetru. Dobro su ustanovljeni mitohondrijski antigeni, antitijela na koje se javlja primarna bilijarna ciroza.
Klinička slika
Primarna bilijarna ciroza trenutno se dijagnosticira u mnogo ranijim fazama nego prethodnih godina (50-60% bolesnika nema kliničke manifestacije u vrijeme dijagnoze). Slabost i pruritus su najčešće rane pritužbe u 21% odnosno 19% bolesnika. Neznatno izraženi simptomi javljaju se kod većine pacijenata u roku od 2-4 godine od početka bolesti, a istodobno oko trećine pacijenata nema dugogodišnje kliničke manifestacije. Slabost je uočena u 78% bolesnika i važan je uzrok invalidnosti. Intenzitet slabosti ne ovisi o stupnju promjena u jetri, a trenutno nema djelotvornih metoda za njegovo liječenje. Pojava svrbeža (u 20-70% slučajeva), u pravilu, je ispred žutice po mjesecima ili godinama. Svrab može biti lokaliziran ili općenit. Obično je izraženije noću i često se povećava u dodiru s vunom i drugim tkivima, kao i toplinom. Uzroci svrbeža nisu poznati, ali endogeni opioidi mogu imati važnu ulogu u njegovom razvoju. Ozbiljnost u desnom hipohondriju prisutna je u oko 10% bolesnika.
Također, bolesnici s primarnom bilijarnom cirozom često doživljavaju hiperlipidemiju, hipotiroidizam, osteopeniju i autoimune bolesti, uključujući Sjogrenov sindrom i sklerodermu. Portalna hipertenzija se obično razvija u kasnim stadijima bolesti, pothranjenosti, nedostatku vitamina topljivih u mastima i steatorrhea - samo u teškim oblicima. U rijetkim slučajevima, pacijenti dolaze s ascitesom, hepatičnom encefalopatijom ili krvarenjem dilatiranih vena jednjaka. Učestalost karcinoma jetre je povećana u bolesnika s dugotrajnom primarnom bilijarnom cirozom. Druge bolesti povezane s primarnom bilijarnom cirozom uključuju intersticijsku upalu pluća, celijakiju, sarkoidozu, bubrežnu tubularnu acidozu, hemolitičku anemiju i autoimunu trombocitopeniju.
Opći pregled bolesnika bez simptoma, u pravilu, ne otkriva obilježja, međutim, kako bolest napreduje, može se pojaviti pigmentacija kože, nevus i grebanje. Xanthelasma je zabilježena u 5-10% bolesnika, a hepatomegalija kod 70%. Splaljinska megalija u ranim stadijima rijetko se primjećuje, ali se može razviti kako bolest napreduje. Žutica je također kasna manifestacija. U uznapredovalim stadijima može doći do atrofije temporalnih i proksimalnih mišića udova, ascitesa i edema.
Za dijagnozu primarne bilijarne ciroze postoje tri kriterija: prisutnost anti-mitohondrijskih protutijela u krvnom serumu, povećanje razine enzima jetre (osobito alkalne fosfataze) više od 6 mjeseci i karakteristične histološke promjene u jetrenom tkivu. Za pretpostavljenu dijagnozu, dvije od tri navedene izmjene su nužne, za konačnu, sve tri. Neki stručnjaci vjeruju da izvođenje biopsije jetre nije potrebno. U isto vrijeme, ove biopsije omogućuju nam da odredimo fazu procesa, kao i pružimo priliku za procjenu učinkovitosti liječenja tijekom vremena. Anti-mitohondrijska protutijela nisu prisutna u 5-10% bolesnika, ali inače nemaju nikakvih razlika u odnosu na klasični oblik bolesti.
Morfološke manifestacije
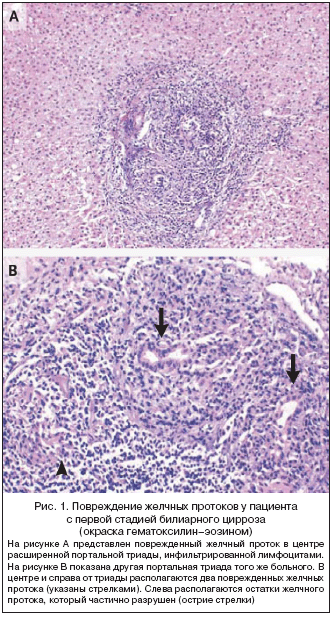
Primarna bilijarna ciroza podijeljena je u četiri histološke faze. Treba napomenuti da čak i prema jednoj biopsiji, pacijent može imati znakove sve četiri faze u isto vrijeme. Istodobno se dijagnoza postavlja na najtežoj od sadašnjih faza. Za primarnu bilijarnu cirozu karakteristična je asimetrična destrukcija žučnih vodova u području portalnih trijada (Slika 1). U prvoj fazi upala je ograničena na područje portalne triade, u drugom se smanjuje broj normalnih žučnih putova, a upalni proces se proteže izvan portalne trijade u okolni parenhim. U trećem stadiju pojavljuju se fibrozni prelazi, koji zajedno spajaju portalne trijade, au četvrtoj fazi tipičnu histološku sliku ciroze s regeneracijskim mjestima.
Klinički tijek i prognoza
Trenutno, pacijenti su značajno vjerojatniji nego prije, u vrijeme postavljanja dijagnoze, nema kliničkih manifestacija. Kao rezultat toga, raniji početak liječenja poboljšava prognozu. Podaci o preživljavanju koji ukazuju na vrlo lošu prognozu dobiveni su u studijama provedenim prije nekoliko desetljeća kada nije bilo djelotvornog liječenja. Sada većina pacijenata s primarnom bilijarnom cirozom dobiva tretman s ursodiolom, a koriste se i drugi lijekovi. Ne manje od 25-30% bolesnika s primarnom bilijarnom cirozom ima visoku učinkovitost ursodiola, karakterizirano normalizacijom biokemijskih parametara i poboljšanjem morfološke slike jetre. Najmanje 20% pacijenata koji primaju ursodiol nemaju histološke znakove progresije bolesti u roku od 4 godine, au nekih čak 10 ili više godina. U nedavnom istraživanju koje je obuhvatilo 262 bolesnika s primarnom bilijarnom cirozom koji su primali ursodiol u prosjeku 8 godina, stopa preživljavanja bolesnika s razinama 1 i 2 bolesti nije se razlikovala od one u općoj populaciji.
Međutim, nisu svi bolesnici s primarnom bilijarnom cirozom otkriveni u ranim stadijima bolesti, pa se stoga učinkovitost liječenja smanjuje. Na primjer, u gore spomenutoj studiji, pacijenti s 3. i 4. stupnjem bolesti imali su značajno povišen (do 2.2) u odnosu na opći populacijski relativni rizik od smrti ili transplantacije jetre, unatoč liječenju ursodiolom. U studiji koja je uključivala 770 pacijenata iz sjeverne Engleske koji su imali dijagnozu primarne bilijarne ciroze od 1987. do 1994. godine, prosječno trajanje život ili vrijeme do transplantacije jetre bilo je samo 9,3 godine, ne prelazeći iznos izračunat za pacijente koji nisu primili liječenje. Nije bilo razlike u očekivanom trajanju života između bolesnika sa i bez kliničkih manifestacija bolesti u vrijeme postavljanja dijagnoze (to nije u skladu s rezultatima drugih studija u kojima su pacijenti bez simptoma imali značajno duži životni vijek). Čimbenici koji su smanjili preživljenje bili su žutica, nepovratni gubitak žučnih putova, ciroza i prisutnost drugih autoimunih bolesti. U dvije studije, prosječno vrijeme do progresije bolesti iz stupnja 1 ili 2 do ciroze u bolesnika koji nisu primali terapiju lijekovima kretali su se od četiri do šest godina. U bolesnika s cirozom razina serumskog bilirubina dosegla je 5 mg / dl (35,5 µmol / L) u oko 5 godina. Niti prisutnost ni titar antimitohondrijskih protutijela nisu bili povezani s napredovanjem bolesti, preživljavanjem bolesnika i djelotvornošću liječenja.
etiologija
Epidemiološki i genetski čimbenici
Primarna bilijarna ciroza je najčešća u sjevernoj Europi. Njegova se učestalost značajno razlikuje u različitim regijama, u rasponu od 40 do 400 milijuna. Primarna bilijarna ciroza je značajno češća kod najbliže rodbine nego u općoj populaciji. Dostupni dokazi upućuju na to da 1-6% pacijenata ima barem jednog člana obitelji koji boluje od ove bolesti (najčešće je takva veza prisutna u parovima majka i kćer i sestri-sestri). Kod monozigotnih blizanaca, podudarnost u odnosu na primarnu bilijarnu cirozu iznosi 63%. U isto vrijeme, za razliku od većine drugih autoimunih bolesti, primarna bilijarna ciroza nije povezana s bilo kojim alelima glavnog kompleksa histokompatibilnosti. Osim toga, uz iznimku povećane učestalosti polimorfizma receptora za vitamin D, drugi genetski čimbenici povezani s povećanom učestalošću primarne bilijarne ciroze nisu identificirani. Omjer žena i muškaraca među pacijentima je 10: 1. Za razliku od skleroderme, primarna bilijarna ciroza nije povezana s poremećenim fetalnim razvojem, ali nedavni podaci ukazuju na to da je prevalencija žena među oboljelim rezultat povećane učestalosti monosomije X kromosoma u limfoidnim stanicama.
Čimbenici okoliša
Molekularna mimikrija je, kao što većina istraživača vjeruje, mogući mehanizam za razvoj autoimunog procesa u bolesnika s primarnom bilijarnom cirozom. Bakterije, virusi i kemikalije mogu biti uzročni čimbenici. Najveće zanimanje je ograničeno na bakterije, prvenstveno na bakteriju Escherichia coli, zbog dostupnosti podataka o povećanoj učestalosti infekcija mokraćnog sustava u bolesnika s primarnom bilijarnom cirozom i stalnosti mitohondrijskih autoantigena. Protutijela humanom kompleksu piruvat dehidrogenaze reagiraju sa sličnim enzimskim kompleksom E. coli.
Proučavali smo gram-negativne tel-bakterije Novo-sphin-go-bium aromaticivorans. Ova bakterija privukla je našu pozornost iz nekoliko razloga: ona je rasprostranjena u okolišu; ima četiri molekule lipoila koje su vrlo slične humanim lipoiliranim autoantigenima; može se otkriti primjenom lančane reakcije polimeraze u oko 20% ljudi; mogu metabolizirati estrogene u aktivni estradiol. U bolesnika s primarnom bilijarnom cirozom, titri antitijela na lipoilne molekule N. aromaticivoransrans su približno 1000 puta viši od onih lipolnih molekula E. coli; Takva se antitijela mogu otkriti i kod pacijenata bez simptoma i kod pacijenata u ranim stadijima bolesti. Uloga drugih bakterija, uključujući laktobacile i klamidije, koje imaju neke strukturne sličnosti s autoantigenima, također se pretpostavlja, međutim, učestalost i titri antitijela za njih su značajno niži od onih za E. coli i N. aromaticivorans. Također je objavljeno da primarna bilijarna ciroza uzrokuje virus iz obitelji retrovirusa, sličan mišjem virusu koji uzrokuje tumore dojke, ali ti podaci nisu potvrđeni.
drugo mogućeg uzroka može doći do izloženosti kemikalijama iz okoliša. Nedavno je pokazano da kemikalije slične piruvat-dehidrogenaza kompleksu vežu protutijela izolirana iz krvnog seruma bolesnika s primarnom bilijarnom cirozom, a afinitet autoantitijela prema tim tvarima često je viši od mitohondrijskih antigena. Mnoge od tih tvari su halogenirani ugljikohidrati, široko rasprostranjeni u prirodi, kao i sadržani u pesticidima i deterdžentima. Jedna od tih supstanci, bromoheksanoatni ester, u kombinaciji s albuminom bikova krvi, uzrokuje pojavu visokih titara antimitohondrijskih antitijela, koja imaju kvantitativne i kvalitativne karakteristike slične antimitohondrijskim protutijelima ljudi. U isto vrijeme, nakon 18 mjeseci, oštećenje jetre kod životinja nije se razvilo. Trenutno nije utvrđeno je li takva kemijska imunizacija važna u razvoju primarne bilijarne ciroze.
Autoimuni odgovor
Anti-mitohondrijska protutijela
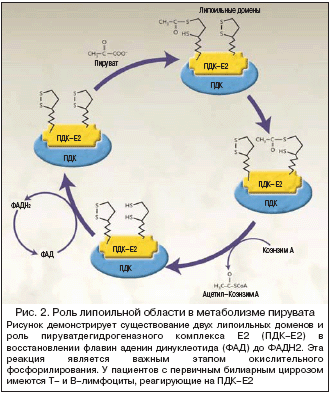
Mitohondrijske antigeni za antitijela su članovi porodice kompleksa oksigenaze 2-okso kiselina, uključujući jedinične E2 kompleks piruvat-dehidrogenaznog kompleksa, 2-okso razgranatu dehidrogenaza kompleksu i digidrolipoamidny ketoglutarata dehidrogenaze za vezanje proteina. Postoje značajne sličnosti između ova četiri autoantigena, osim toga, svi oni sudjeluju u oksidativnoj fosforilaciji i sadrže lipoičnu kiselinu. U većini slučajeva, antitijela reagiraju s kompleksom E2 piruvat dehidrogenaze (PDK-E2). Svi se antigeni nalaze u unutarnjem mitohondrijskom matriksu i kataliziraju oksidacijsku dekarboksilaciju keto kiselina (slika 2). Enzimi iz skupine E2 imaju zajedničku strukturu. Periferni dio ovih enzima je odgovoran za vezanje El i E3 komponenti jedni za druge, dok C-kraj na kojem se nalazi aktivni centar obavlja aktivnost acil transferaze.
Općenito, MPC-E2 je velika višedimenzionalna struktura koja se sastoji od oko 60 elemenata međusobno povezanih. Njegova veličina prelazi veličinu ribosoma, a za metabolizam piruvata potrebna je lipoična kiselina. Primarna bilijarna ciroza je jedina bolest u kojoj su otkrivene T i B stanice koje reagiraju s MPC-E2. Nekoliko studija koje su koristile oligopeptide i rekombinantne proteine pokazale su da se glavni epitop na koji se vežu antimitohondrijska antitijela nalazi u području lipoilnih skupina. Osim toga, kada se koriste rekombinantni autoantigeni u dijagnostičke svrhe, otkrivanje antimitohondrijskih antitijela omogućuje vam nedvosmisleno utvrđivanje dijagnoze primarne bilijarne ciroze, ili barem ukazuje na to da osoba ima značajno povećan rizik od razvoja primarne bilijarne ciroze u sljedećih nekoliko godina. 5-10 godina. Iako su anti-mitohondrijska protutijela dominantni oblik autoantitijela u primarnoj bilijarnoj cirozi, gotovo svi bolesnici imaju povišene razine imunoglobulina M.
Iako je mehanizam uništenja bilijarnog trakta i dalje nejasan, specifičnost patoloških promjena u bilijarnom traktu, prisutnost infiltracije limfocita u području portalnog trakta i prisutnost histokompatibilnosti II. , Postoji dovoljno dokaza da se uništavanje žučnih putova uglavnom provodi autoreaktivnim T-limfocitima.
Antimitohondrijski T limfociti
T-limfociti koji infiltriraju jetru u primarnoj bilijarnoj cirozi specifični su za MPC-E2. Štoviše, učestalost pojavljivanja prekursora autoreaktivnih CD4 + T-limfocita u jetri i regionalnim limfnim čvorovima je 100-150 puta veća od one u krvotoku. Sadržaj CD8 + T-limfocita, prirodnih stanica ubojica i B-limfocita, koji reagiraju s MPC-E2, također je veći u jetri u odnosu na krv. Detaljna studija MPC-E2 molekule pokazala je da su aminokiseline od 163 do 176 epitop za T-limfocite. Ovo mjesto se nalazi u području lipoilnih elemenata i na istom mjestu gdje se autoantitijela vežu za MPC-E2 molekulu. Autoreaktivni T-limfociti imaju receptore CD4, CD45RO, kao i receptore za T-limfocite iz a / b grupe, i međusobno djeluju s HLA-DR53. Detaljnije studije su pokazale da su aminokiseline E, D i K na pozicijama 170, 172 i 173, nužno za autoimune T-limfocite da se vežu na molekule MPC-E2. Od posebnog interesa je aminokiselina K (lizin), koja veže lipoičnu kiselinu.
Lipoična kiselina ima disulfidnu vezu, koja se lako uništava, nalazi se na površini molekule. Autoreaktivni T limfociti periferne krvi koji reagiraju s jednim epitopom otkriveni su samo u bolesnika s ranim stadijima bolesti, što ukazuje da se s porastom bolesti broj autoantigena povećava. Uporaba tetramera glavnog kompleksa histokompatibilnosti klase I pokazala je da su CD8 + T-limfociti specifični za MPC-E2 10-15 puta češći u jetri u usporedbi s krvlju. Detaljno proučavanje epitopa za HLA-A * 0201 pokazalo je vezanje za MAC max-E2 aminokiseline od 165 do 174, tj. Na isto mjesto na koje se vežu autoantitijela i T-limfociti. Ovi podaci ponovno ukazuju na lipoilne elemente i lipoičnu kiselinu kao najvažnija vezna mjesta.
Stanice žučnog kanala i apoptoza
Glavni paradoks povezan s primarnom bilijarnom cirozom je da su mitohondrijski proteini prisutni u svim stanicama koje imaju jezgre, dok u isto vrijeme autoimuni proces utječe samo na epitel žučnih putova. U tom smislu, važne su razlike u metabolizmu MPC-E2 tijekom apoptoze u stanicama žučnih kanala i kontrolnim stanicama. Tri najnovija otkrića koja se odnose na te razlike posebno su važna za razumijevanje primarne bilijarne ciroze. Jedna od tih činjenica je da stanje stanice, naime, da li je lizin-lipilna regija E2 proteina izmijenjena glutationom tijekom apoptoze, određuje mogućnost pojave autoantitijela na MPC-E2. Sljedeća činjenica je da se metabolizam PDK-E2 u epitelnim stanicama razlikuje od metabolizma u drugim stanicama tijela - tijekom apoptoze glutation se ne veže za lizin-lipoil regiju. Konačno, specifične modifikacije unutarnjeg lizin-lipoilnog područja MPC-E2 pod djelovanjem ksenobiotika dovele su do pojave imunološke reaktivnosti na serum pacijenata, što još jednom naglašava važnost stanja lizin-lipoil regije. Ovi podaci pokazuju da stanice žučnih kanala nisu samo “žrtve” autoimunog procesa. Naprotiv, oni sami uzrokuju autoimuni proces kao posljedica osobitosti metabolizma MPC-E2. Također treba napomenuti da stanice žučnih kanala sintetiziraju poliimunoglobulinski receptor, koji može biti drugi mehanizam za razvoj autoimunog procesa.
Antinuklearna antitijela
Autoantitijela na nuklearne antigene otkrivena su u približno 50% bolesnika s primarnom bilijarnom cirozom, a često i kod pacijenata koji nemaju antimitohondrijska antitijela. Najčešće, antitijela formiraju prsten oko jezgre, kao i mnoga mjesta nastala autoantitijelima na GP210 i nukleoporin 62 u području nukleopora, kao i na nuklearni protein sp100. Ovaj raspored antitijela je izuzetno specifičan za ovu bolest.
Liječenje simptoma i komplikacija
svrabež
Tablica 1 prikazuje lijekove koji se koriste za liječenje pruritusa u bolesnika s primarnom bilijarnom cirozom.
osteoporoza
Osteoporoza se razvija u oko trećine bolesnika. Međutim, teški oblici, koji često dovode do prijeloma kostiju, sada su rijetki. Trenutno nema liječenja koštanih lezija u primarnoj bilijarnoj cirozi, osim transplantacije jetre. Osteopenija se može pogoršati tijekom prvih šest mjeseci nakon transplantacije, međutim, mineralna gustoća kosti se vraća na početnu vrijednost nakon 12 mjeseci i dalje se poboljšava. Alendronat može povećati mineralnu gustoću kostiju, ali nema dokaza o njegovoj dugoročnoj učinkovitosti. Estrogenska nadomjesna terapija može smanjiti ozbiljnost osteoporoze u žena u postmenopauzi.
hiperlipidemija
Krvni lipidi mogu se značajno povećati u bolesnika s primarnom bilijarnom cirozom, ali rizik od smrti od aterociroze se ne povećava. U većini slučajeva uporaba lijekova koji smanjuju kolesterol nije potrebna, međutim, prema našem iskustvu, statini i ezetimib su potpuno sigurni.
Portalna hipertenzija
Za razliku od pacijenata s drugim bolestima jetre, kod kojih se krvarenje iz dilatiranih vena jednjaka obično razvija u kasnijim fazama, u bolesnika s primarnom bilijarnom cirozom, ova se komplikacija često javlja u ranim fazama, prije samog razvoja žutice ili same ciroze. Trenutno je endoskopsko ligiranje i transjugularno intrahepatično portosistemsko skretanje sa stentiranjem zamijenjeno distalnim splenorenalnim ranžiranjem. Pacijenti mogu živjeti mnogo godina nakon krvarenja bez transplantacije jetre.
Liječenje osnovne bolesti
Ursodeoksiholna kiselina
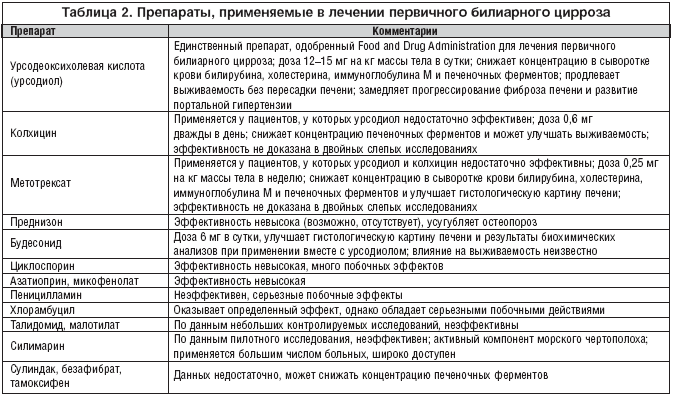
Ursodeoxycholic kiselina (ursodiol), koja je epimer chenodeoxycholic kiselina, je 2% ljudskih žučnih kiselina i ima choleretic aktivnost. Ursodiol u dozi od 12 do 15 mg po kg tjelesne težine je jedini lijek koji je odobrila Uprava za hranu i lijekove za liječenje primarne bilijarne ciroze (Tablica 2). Smanjuje razinu bilirubina, alkalne fosfataze, alanin aminotransferaze, aspartat aminotransferaze, kolesterola i imunoglobulina M u serumu. Prema radu, u kojem su kombinirani rezultati tri kontrolirane studije, koji obuhvaća ukupno 548 bolesnika, ursodiol je značajno smanjio vjerojatnost transplantacije ili smrti jetre u roku od četiri godine. Ursodiol je siguran i ima malu količinu nuspojava. Kod nekih bolesnika zabilježeni su porast tjelesne težine, gubitak kose te u rijetkim slučajevima proljev i nadutost. Ursodiol je i dalje učinkovit u liječenju 10 godina. On usporava progresiju fibroze jetre u ranoj primarnoj bilijarnoj cirozi i razvoju varikoziteta jednjaka, ali je neučinkovit u kasnijim fazama bolesti.
Ursodiol usporava stopu progresije bolesti u većine bolesnika i vrlo je učinkovit u 25-30% bolesnika. Očekivano trajanje života bolesnika liječenih ursodiolom bilo je slično kao u sličnoj dobnoj skupini zdravih ljudi kada je promatrana 20 godina. Međutim, bolest je često napredovala, što je zahtijevalo postavljanje dodatnih lijekova.
Kolhicin i metotreksat
Ovi lijekovi se dugo koriste u liječenju primarne bilijarne ciroze, iako njihova uloga nije potpuno jasna. Kolhicin smanjuje serumsku alkalnu fosfatazu, serum alanin aminotransferaze i aspartat aminotransferaze prema nekoliko dvostruko slijepih prospektivnih studija, ali je manje učinkovit od ursodiola. Kolhicin smanjuje intenzitet pruritusa, prema dvije studije, i poboljšava histološku sliku jetre, prema trećem, dok kolhicin nije bio učinkovit u još jednom radu. Nedavna meta-analiza pokazala je da kolhicin smanjuje učestalost teških komplikacija, ciroze i povećava vrijeme do transplantacije jetre.
U malim dozama koje se koriste u liječenju primarne bilijarne ciroze (0,25 mg po kilogramu tjedno oralno), metotreksat može imati imunomodulatorni, a ne anti-metabolički učinak. Prema nekim istraživanjima, metotreksat poboljšava biokemijske parametre i histološku sliku jetre kada se kombinira s ursodiolom u bolesnika s nedovoljnom djelotvornošću. Primjena metotreksata dovela je do perzistentne remisije u nekih bolesnika s prekirrotičnom primarnom bilijarnom cirozom. U isto vrijeme, u drugim studijama, primjena metotreksata kao monoterapije, kao iu kombinaciji s ursodiolom, nije bila učinkovita. Štoviše, prema 10-godišnjoj studiji objavljenoj 2004. godine, stopa preživljavanja pacijenata koji su primili metotreksat i ursodiol bila je ista kao i kod onih koji su primali kolhicin i ursodiol i odgovarali su prognozi temeljenoj na modelu Mayo. U trećini bolesnika nakon 10 godina liječenja broj simptoma primarne bilijarne ciroze bio je mali. Niti jedan od pacijenata koji su bili na prekirrotičnoj fazi prije početka liječenja nije razvio cirozu. Metotreksat može uzrokovati intersticijsku pneumoniju, sličnu onoj u bolesnika s reumatoidnim artritisom.
Ostali lijekovi
Budesonid poboljšava biokemijske parametre i smanjuje ozbiljnost morfoloških promjena kada se koristi u kombinaciji s ursodiolom, ali može pogoršati osteopeniju. Prednizolon je neučinkovit i povećava učestalost osteoporoze. Silymarin, aktivna komponenta morskog čička, neučinkovit je. Besafibrat (derivat fibrata koji se koristi u liječenju hiperkolesterolemije) poboljšava biokemijske parametre, a tamoksifen smanjuje razinu alkalne fosfataze kod dvije žene koje su ga uzele nakon kirurškog liječenja raka dojke. Sulindak je poboljšao biokemijske parametre u kombinaciji s ursodiolom. Drugi lijekovi koji su, prema istraživanjima, ili neučinkoviti ili toksični, uključuju klorambucil, penicilamin, azatioprin, ciklosporin, malotilat, talidomid i mofetilmikofenolat.
Transplantacija jetre
Transplantacija jetre može značajno produžiti život bolesnika s bilijarnom cirozom i jedino je učinkovito liječenje bolesnika s zatajenjem jetre. Stope preživljavanja su 92, odnosno 85% u godini i pet godina. Većina bolesnika ne pokazuje znakove oštećenja jetre nakon operacije, ali ostaju anti-mitohondrijska protutijela. Primarna bilijarna ciroza se ponavlja u roku od 3 godine u 15% bolesnika i unutar 10 godina u 30%.
Rasprava o liječenju
Optimalno liječenje primarne bilijarne ciroze još nije utvrđeno. Pristup za svakog pacijenta mora biti individualan. Liječenje započinje s ursodiolom. Kolhicin se dodaje ako je djelotvornost liječenja ursodiolom tijekom godine nedovoljna. Ako kombinacija ursodiola i kolhicina također nije dovoljno učinkovita u liječenju godinu dana, dodajte metotreksat. Liječenje se smatra učinkovitim u nestanku svraba, smanjujući razinu alkalne fosfataze na vrijednosti koje prelaze normu za ne više od 50%, kao i za poboljšanje histološkog uzorka prema biopsiji jetre. Metotreksat se prekida ako nema učinka u roku od godinu dana. Najvjerojatniji pozitivni učinak primjene kolhicina i metotreksata u bolesnika s povećanjem razine alkalne fosfataze pet ili više puta u usporedbi s normom i intenzivnom portalnom i periportalnom upalom.
Pravci budućeg istraživanja
Nedostatak životinjskog modela primarne bilijarne ciroze je prepreka za proučavanje ove bolesti. Istraživanja na ljudima bila su usmjerena na objašnjavanje činjenice da antitijela na široko rasprostranjene mitohondrijske antigene utječu samo na epitel bilijarnog trakta. Istraživanja su pokazala da post-translacijska modifikacija PDK-E2 dovodi do smanjene percepcije ovog proteina od strane imunološkog sustava. Moguće je, na primjer, da je kršenje metabolizma lizin-lipoata u tim mitohondrijskim antigenima najvažniji mehanizam koji vodi razvoju autoimune reakcije. Također je vjerojatno da ova reakcija dalje uključuje epitel bilijarnog trakta zbog jedinstvenih biokemijskih svojstava žučnih putova, uključujući prisutnost poliimunoglobulinskog receptora na epitelnim stanicama i karakteristike njihove apoptoze.
Sažetak izradio V.V. Iremashvili na temelju članaka Kaplana M.M., Gershwina M.E. Primarna bilijarna ciroza, New England Journal of Medicine 2005;
Ne. 353: str. 1261-1273.
književnost
1. Gershwin ME, Mackay IR, Sturgess A, Coppel RL. Identifikacija i specifičnost cDNA koja kodira 70 kd mitohondrijski antigen prepoznata u bilijarnoj cirozi. J Immunol 1987; 138: 3525-31.
Kaplan MM. Primarna bilijarna ciroza. N Engl J Med 1996; 335: 1570-80.
3. Pares A, Rodes J. Prirodna povijest primarne bilijarne ciroze. Clin Liver Dis 2003; 7: 779-94.
4. Princ MI, Chetwynd A, Craig WL, Metcalf JV, James OF. Asimptomatska primarna bilijarna ciroza: klinička slika, prognoza i progresija simptoma u velikoj populacijskoj kohorti. Gut 2004; 53: 865-70.
5. Bergasa NV. Pruritus i umor u primarnoj bilijarnoj cirozi. Clin Liver Dis 2003; 7: 879-900.
6. Princ M, Chetwynd A, Newman W, Metcalf JV, James OFW. Preživljavanje i progresija simptoma u velikoj zemljopisnoj skupini bolesnika s primarnom bilijarnom cirozom: praćenje do 28 godina. Gastroenterology 2002; 123: 1044-51.
7. Milkiewicz P, Heathcote EJ. Umor kod kronične kolestaze. Gut 2004; 53: 475-7.
8. Forton DM, Patel N, Prince M, et al. Povezanost omjera prijenosa magnetizacije globusa i razine mangana u krvi. Gut 2004; 53: 587-92.
9. Poupon RE, Chretien Y, Chazouilleres O, Poupon R, Chwalow J. Hepatology 2004; 40: 489-94.
Talwalkar JA, Souto E, Jorgensen RA, Lindor KD. Prirodna povijest svrbeža u primarnoj bilijarnoj cirozi. Clin Gastroenterol Hepatol 2003; 1: 297-302.
11. Laurin JM, DeSotel CK, Jorgensen RA, Dickson ER, Lindor KD. Biliarna ciroza povezana s primarnom bilijarnom cirozom. Am J Gastroenterol 1994; 89: 1840-3.
12. Watt FE, James OF, Jones DE. Uzorci autoimune bolesti u bolesnika s primarnom bilijarnom cirozom i njihovih obitelji: populacijska kohortna studija. QJM 2004; 97: 397-406.
13. Nakanuma Y. Je li esophagogastric varijacija u primarnoj bilijarnoj cirozi? J Gastroenterol 2003; 38: 1110-2.
14. Nijhawan PK, Thernau TM, Dickson ER, Boynton J, Lindor KD. Incident bilijarne ciroze: iskustvo Mayo. Hepatology 1999; 29: 1396-8.
15. Princ MI, James OF. Epidemiologija primarne bilijarne ciroze. Clin Liver Dis 2003; 7: 795-819.
16. Poupon RE, Lindor KD, Pares A, Chazouilleres O, Poupon R, Heathcote EJ. Kombinirana analiza liječenja ursodeoksiholne kiseline u primarnoj bilijarnoj cirozi. J Hepatol 2003; 39: 12-6.
17. Poupon R. Ispitivanja primarne bilijarne ciroze: potreba za pravim lijekovima u pravo vrijeme. Hepatology 2004; 39: 900-2.
Lee YM, Kaplan MM. Učinkovitost kolhicina u bolesnika s primarnom bilijarnom cirozom slabo reagira na ursodiol i metotreksat. Am J Gastroenterol 2003; 98: 205-8.
Kaplan MM, DeLellis RA, Wolfe HJ. Održana biokemijska i bilijarna ciroza kao odgovor na liječenje. Ann Intern Med 1997; 126: 682-8.
20. Bonis PAL, Kaplan M. Metotreksat poboljšao je biokemijske testove u bolesnika s primarnom bilijarnom cirozom koji nepotpuno reagiraju na ursodiol. Gastroenterology 1999; 117: 395-9.
21. Leuschner M, Dietrich CF, Vi T, et al. Karakterizacija bolesnika s primarnom bilijarnom cirozom koji reagiraju na dugotrajno liječenje ursodeoksiholnom kiselinom. Gut 2000; 46: 121-6.
22. Locke GR III, Therneau TM, Ludwig J, Dickson ER, Lindor KD. Vremenski tijek histološke progresije u primarnoj bilijarnoj cirozi. Hepatology 1996; 23: 52-6.
23. Corpechot C, Carrat F, Bahr A, Chretien Y, Poupon R-E, Poupon R. Bilijarna ciroza. Gastroenterology 2005; 128: 297-303.
24. Degott C, Zafrani ES, Callard P, Balkau B, Poupon RE, Poupon R. Histopatološka studija bilijarne ciroze i liječenje ursodeoksiholne kiseline na histološkoj progresiji. Hepatology 1999; 29: 1007-12.
25. Therneau TM, Grambsch PM. Modeliranje podataka o preživljavanju: proširenje Cox modela. New York: Springer, 2000: 261-87.
26. Heathcote EJ, Cauch-Dudek K, Walker V i sur. Kanadska multicentrična dvostruka randomizirana kontrolna studija ursodeoksiholne kiseline u primarnoj bilijarnoj cirozi. Hepatology 1994; 19: 1149-56.
27. Poupon RE, Lindor KD, Cauch-Dudek K, Dickson ER, Poupon R, Heathcote EJ. Kombinirana analiza randomiziranih kontroliranih ispitivanja ursodeoksiholne kiseline u primarnoj bilijarnoj cirozi. Gastroenterology 1997; 113: 884-90.
28. Springer J, Cauch-Dudek K, O'Rourke K, Wanless I, Heathcote EJ. Asimptomatska primarna bilijarna ciroza: proučavanje prirodne povijesti i prognoze. Am J Gastroenterol 1999; 94: 47-53.
29. Corpechot C, Carrat F, Bonn i AM, Poupon RE, Poupon R. Bilijarna ciroza. Hepatology 2000; 32: 1196-9.
30. Van Norstrand MD, Malinchoc M, Lindor KD, i sur. Kvantitativno mjerenje autoantitijela na rekombinantne mitohondrijske antigene u bolesnika s primarnom bilijarnom cirozom: Hepatology 1997; 25: 6-11.
31. Parikh-Patel A, zlatni EB, Worman H, Krivy KE, Gershwin ME. Čimbenici rizika za primarnu bilijarnu cirozu u skupini bolesnika iz Sjedinjenih Država. Hepatology 2001; 33: 16-21.
32. Howel D, Fischbacher CM, Bhopal RS, Gray J, Metcalf JV, James OF. Istraživačka studija slučaja i kontrole primarne bilijarne ciroze na temelju populacije. Hepatology 2000; 31: 1055-60.
33. Sood S, Gow PJ, Christie JM, Angus PW. Epidemiologija primarne bilijarne ciroze u Viktoriji, Australija: visoka prevalencija u populaciji migranata. Gastroenterology 2004; 127: 470-5.
34. Bittencourt PL, Farias AQ, Abrantes-Lemos CP, i sur. Bolesnici s primarnom bilijarnom cirozom. J Gastroenterol Hepatol 2004; 19: 873-8.
35. Selmi C, Mayo MJ, Bach N, et al. Primarna bilijarna ciroza kod monozigotnih i dizigotnih blizanaca: genetika, epigenetika i okoliš. Gastroenterology 2004; 127: 485-92.
36. Invernizzi P, Battezzati PM, Crosignani A, et al. Osobni polimorfizmi HLA u talijanskih bolesnika s primarnom bilijarnom cirozom. J Hepatol 2003; 38: 401-6.
37. Jones DE, Donaldson PT. Genetski čimbenici u patogenezi primarne bilijarne ciroze. Clin Liver Dis 2003; 7: 841-64.
38. Springer JE, Cole DE, Rubin LA, i sur. Genotipovi receptora vitamina D bilijarne ciroze. Gastroenterology 2000; 118: 145-51.
39. Tanaka A, Lindor K, Gish R, et al. Samo mikročimerizam fetusa ne doprinosi indukciji primarne bilijarne ciroze. Hepatology 1999; 30: 833-8.
40. Invernizzi P, Miozzo M, Battezatti PM, i sur. Učestalost monosomije X u žena s primarnom bilijarnom cirozom. Lancet 2004; 363: 533-5.
41. Selmi C, Gershwin EM. Bakterije i ljudska autoimunost: slučaj primarne bilijarne ciroze. Curr Opin Rheumatol 2004; 16: 406-10.
42. Selmi C, Balkwill DL, Invernizzi P, et al. Bolesnici s primarnom bilijarnom cirozom reagiraju protiv sveprisutne bakterije koja metabolizira ksenobiotike. Hepatology 2003; 38: 1250-7.
43. XuL, Shen Z, Guo L, et al. Je li bilivirusna infekcija bilijarne ciroze? Proc Natl Acad Sci U 2003; 100: 8454-9.
44. Selmi C, Ross SA, Ansari A, i sur. Nedostatak luminoznog ili retrovirusnog miša kod primarne bilijarne ciroze. Gastroenterology 2004; 127: 493-501.
45. Long SA, Quan C, Van de Water J, et al. Imunoreaktivnost organske komponente E2 piruvat dehidrogenaze: povezivanje ksenobiotika s primarnom bilijarnom cirozom. J Immunol 2001; 167: 2956-63.
46. Leung PS, Quan C, Park O, et al. Imunizacija s konjugatom ksenobiotskog 6-bromoheksan goveđeg serumskog albumina inducira antimitohondrijska antitijela. J Immunol 2003; 170: 5326-32.
47. Bruggraber SF, Leung PS, Amano K, i sur. Autoreaktivnost prema lipoatu i konjugiranoj bilijarnoj cirozi. Gastroenterology 2003; 125: 1705-13.
48. Gershwin ME, Ansari AA, Mackay IR, i sur. Primarna bilijarna ciroza: orkestrirani imunološki odgovor protiv epitelnih stanica. Immunol Rev 2000; 174: 210-25.
49. Kita H, Matsumura S, He X-S, et al. Specifična autoreaktivna citotoksična analiza limfocita u primarnoj bilijarnoj cirozi. J Clin Invest 2002; 109: 1231-40.
50. Kita H, Naidenko OV, Kronenberg M, et al. Analiza prirodnih stanica ubojica stanica u primarnoj bilijarnoj cirozi pomoću ljudskog CD1d tetramera. Gastroenterology 2002; 123: 1031-43.
51. Shimoda S, Van de Water J, Ansari A, i sur. Identifikacija motiva epitopa stanica kod mitohondrijskih autoantigena u primarnoj bilijarnoj cirozi. J Clin Invest 1998; 102: 1831-40.
52. Odin JA, Huebert RC, Casciola-Rosen L, LaRusso NF, Rosen A. Bcl-2-ovisna oksidacija piruvat dehidrogenaze-E2, autoantigen primarne bilijarne ciroze, tijekom apoptoze. J Clin Invest 2001; 108: 223-32.
53. Amano K, Leung PS, Xu Q, i sur. Biliarna ciroza je reverzibilna. J Immunol 2004; 172: 6444-52.
54. Matsumura S, Kita H, He XS, i sur. Sveobuhvatno mapiranje epitopa H8-A0201-ograničenih CD8 T-stanica na PDC-E2 u primarnoj bilijarnoj cirozi. Hepatology 2002; 36: 1125-34.
55. Worman HJ, Courvalin JC. Antinuklearna antitijela specifična za primarnu bilijarnu cirozu. Autoimmun Rev 2003; 2: 211-7.
56. Ghent CN, Carruthers SG. Liječenje pruritusa u primarnoj bilijarnoj cirozi s rifampinom: rezultati dvostruko slijepog, križnog, randomiziranog ispitivanja. Gastroenterology 1988; 94: 488-93.
57. Cohen LB, Ambinder EP, Wolke AM, Field SP, Schaffner F. Uloga plazmafereze u primarnoj bilijarnoj cirozi. Gut 1985; 26: 291-4.
58. Levy C, Lindor KD. Liječenje osteoporoze, nedostatak vitamina topivih vitamina i hiperlipidemija kod primarne bilijarne ciroze. Clin Liver Dis 2003; 7: 901-10.
59. Ormarsdottir S, Ljunggren O, Mallmin H, Olsson R, Prytz H, Loof L. Uzdužni gubitak kosti kod žena u postmenopauzi s primarnom bilijarnom cirozom i dobro očuvanom funkcijom jetre. J Med Med 2002; 252: 537-41.
60. Boulton-Jones JR, Fenn RM, West J, Logan RF, Ryder SD. Ciroza bicikla: nema povećanja u usporedbi s općom populacijskom kontrolom. Aliment Pharmacol Ther 2004; 20: 551-7.
61. Guanabens N, Pares A, Ros I, et al. Važno je da pacijenti s primarnom bilijarnom cirozom mogu poboljšati razinu koštane srži. Am J Gastroenterol 2003; 98: 2268-74.
62. Menon KV, Angulo P, GM GM, Lindor KD. Biliarna ciroza. Am J Gastroenterol 2003; 98: 889-92.
63. Longo M, Crosignani A, Battezzati PM, i sur. Hiperlipidemično stanje i kardiovaskularni rizik bilijarne ciroze. Gut 2002; 51: 265-9.
64. Thornton JR, Triger DR. Varicealno krvarenje povezano je sa smanjenom kolestazom u primarnoj bilijarnoj cirozi. Q J Med 1989; 71: 467-71.
Boyer TD, Kokenes DD, Hertzler G, Kutner MH, Henderson JM. Utjecaj distalnog splanorenalnog šanta na bolesnike s primarnom bilijarnom cirozom. Hepatology 1994; 20: 1482-6.
66. Pares A, Caballeria L, Rodes J, i sur. Ursodeoksiholna kiselina u primarnoj bilijarnoj cirozi: rezultati dvostruko slijepog kontroliranog multicentričnog ispitivanja. J Hepatol 2000; 32: 561-6.
67. Poupon RE, Bonnand AM, Chretien Y, Poupon R. Desetogodišnje preživljavanje u pacijenata liječenih primarnom bilijarnom cirozom ursodeoksiholne kiseline. Hepatology 1999; 29: 1668-71.
68. Lindor KD, Jorgenson RA, Therneau TM, Malinchoc M, Dickson ER. Ursodeoksiholna kiselina odgađa nastanak varikoziteta jednjaka u primarnoj bilijarnoj cirozi. Mayo Clin Proc 1997; 72: 1137-40.
69. Goulis J, Leandro G, Burroughs AK. Randomizirana kontrolirana ispitivanja terapije ursodeoksiholnom kiselinom za primarnu bilijarnu cirozu: meta-analiza. Lancet 1999; 354: 1053-60.
70. Gluud C, Christensen E. Ursodeoksiholna kiselina za primarnu bilijarnu cirozu. Cochrane Database Syst Rev 2002; 1: CD000551.
71. Corpechot C, Carrat F, Bahr A, Poupon RE, Poupon R. Utjecaj ursodeoksiholika (UDCA) na dugoročno preživljavanje bilijarne ciroze. Hepatology 2003; 34: 519A. sažetak.
72. Kaplan MM, Alling DW, Zimmerman HJ, i sur. Prospektivno ispitivanje kolhicina za primarnu bilijarnu cirozu. N Engl J Med 1986; 315: 1448-54.
73. Vuoristo M, Farkkila M, Karvonen AL, et al. U placebo-kontroliranom pokusu liječenja primarne bilijarne ciroze kolhicinom i ursodeoksiholnom kiselinom. Gastroenterology 1995; 108: 1470-8.
74. Kaplan MM, Schmid C, Provenzale D, Sharma A, Dickstein G, McKusick A. Test prospektivne kolikarne ciroze. Gastroenterology 1999; 117: 1173-80.
75. Kaplan MM, Cheng S, Cijena LL, Bonis PA. Randomizirano kontrolirano ispitivanje kolhicina plus ursodiola u odnosu na metotreksat plus ursodiol u primarnoj bilijarnoj cirozi: rezultati desetogodišnjeg. Hepatology 2004; 39: 915-23.
76. Almasio P, Floreani A, Chiaramonte M, et al. Multicentrično randomizirano, placebo kontrolirano ispitivanje ursodeoksiholne kiseline s bilijarnom cirozom. Aliment Pharmacol Ther 2000; 14: 1645-52.
77. Vela S, Agrawal D, Khurana S, Singh P. Kolhicin za primarnu bilijarnu cirozu: meta-analiza prospektivnih kontroliranih ispitivanja. Gastroenterology 2004; 126: A671-A672. sažetak.
78. Cronstein BN, Naime D, Ostad E. Protuupalni mehanizam metotreksata povećan oslobađanjem adenozina na upalnim mjestima smanjuje akumulaciju leukocita in vivo modelom upale. J Clin Invest 1993; 92: 2675-82.
79. Hendrickse M, Rigney E, Giaffer MH i sur. Niske doze metotreksata dugoročni su rezultati placebo kontroliranog ispitivanja. Gastroenterology 1999; 117: 400-7.
Gonzalez-Koch A, Brahm J, Antezana C, Smok G, Cumsille MA. Kombinacija ursodeoksiholne kiseline i metotreksata za primarnu bilijarnu cirozu nije bolja od same ursodeoksiholne kiseline. J Hepatol 1997; 27: 143-9.
81. Combes B, Emerson SS, Flye NL. Primarna bilijarna ciroza (PBC) ursodiol (UDCA) plus metotreksat (MTX) ili placebo studija (PUMPS) - multicentrično randomizirano ispitivanje. Hepatology 2003; 38: 210A. sažetak.
82. Leuschner M, Maier KP, Schlictling J, et al. Oralni budesonid i ursodeoksiholna kiselina za liječenje primarne bilijarne ciroze: rezultati prospektivnog dvostruko slijepog ispitivanja. Gastroenterology 1999; 117: 918-25.
83. Rautiainen H, Karkkainen P, Karvonen AL, et al. Budesonid u kombinaciji s UDCA poboljšava histologiju jetre u bilijarnoj cirozi: trogodišnje randomizirano ispitivanje. Hepatology 2005; 41: 747-52.
84. Angulo P, Jorgensen RA, Keach JC, Dickson ER, Smith C, Lindor KD. Oralni budezonid u bolesnika s bilijarnom cirozom s suboptimalnim odgovorom na ursodeoksiholnu kiselinu. Hepatology 2000; 31: 318-23.
85. Mitchison HC, Palmer JM, Bassendine MF, Watson AJ, Record CO, James OF. Kontrolirano ispitivanje prednizolona u primarnoj bilijarnoj cirozi: trogodišnji rezultati. J Hepatol 1992; 15: 336-44.
86. Angulo P, Patel T, Jorgensen RA, Therneau TM, Lindor KD. Silymarin u liječenju bolesnika s primarnom bilijarnom cirozom s suboptimalnim odgovorom na ursodeoksiholnu kiselinu. Hepatology 2000; 32: 897-900.
87. Nakai S, Masaki T, Kurokohchi K, Deguchi A, Nishioka M., Kombinirana terapija za primarnu bilijarnu cirhozu: preliminarna studija. Am J Gastroenterol 2000; 95: 326-7.
88. Reddy A, princ M, James OF, Jain S, Bassendine MF. Tamoxiphen: novo liječenje primarne bilijarne ciroze? Liver Int 2004; 24: 194-7.
89. Leuschner M, Holtmeier J, Ackermann H, Leuschner U. Pilot studija. Eur J Gastroenterol Hepatol 2002; 14: 1369-76.
90. Hoofnagle JH, Davis GL, Schafer DF, i sur. Randomizirano ispitivanje klorambucila za primarnu bilijarnu cirozu. Gastroenterology 1986; 91: 1327-34.
91. James OF. D-penicilamin za primarnu bilijarnu cirozu. Gut 1985; 26: 109-13.
92. Christensen E, Neuberger J, Crowe J, et al. Konačni učinak međunarodnog suđenja. Gastroenterology 1985; 89: 1084-91.